FLEXIBLE DOSIERUNG
EMPFOHLENES DOSIERUNGSSCHEMA1
| LGS | DS | TSC | |
|---|---|---|---|
| Erste Woche | Anfangsdosis 5 mg/kg/Tag (zweimal täglich je 2,5 mg/kg) | ||
| Zweite Woche | Erhaltungsdosis 10 mg/kg/Tag (zweimal täglich je 5 mg/kg) | 10 mg/kg/Tag (zweimal täglich je 5 mg/kg) | |
| Weitere Titration je nach Bedarf (schrittweise) | Wöchentliche Erhöhung um 5 mg/kg/Tag (zweimal täglich je 2,5 mg/kg) | ||
| Empfohlene Höchstdosis | 20 mg/kg/Tag (zweimal täglich je 10 mg/kg) | 25 mg/kg/Tag (zweimal täglich je 12,5 mg/kg) | |
Je nach individuellem klinischem Ansprechen und Verträglichkeit sollte die Titration schrittweise in Gaben von je 2,5 mg/kg/Tag erfolgen (5 mg/kg/Tag).
Dosissteigerungen von mehr als 10 mg/kg/Tag bis zur empfohlenen Höchstdosis sollten nur nach sorgfältiger individueller Nutzen-Risiko-Abwägung und unter strenger Überwachung erfolgen.1
Behandlungsabbruch
Falls EPIDYOLEX® abgesetzt werden muss, sollte die Dosis allmählich reduziert werden. In klinischen Studien wurde EPIDYOLEX® schrittweise 10 Tage lang um jeweils 10% pro Tag reduziert. Eine langsamere bzw. schnellere Dosisverringerung liegt je nach klinischer Notwendigkeit im Ermessen des behandelnden Arztes.1
Bei Patienten mit leichter Leberfunktionsstörung bzw. leichter, mittelschwerer oder schwerer Nierenfunktionsstörung ist keine Dosisanpassung von EPIDYOLEX® erforderlich.1
OPTIMIERTES ANSPRECHEN
EPIDYOLEX® kann mit anderen Anfallssuppressiva und Arzneimitteln gegeben werden (ggf. Dosisanpassung).1
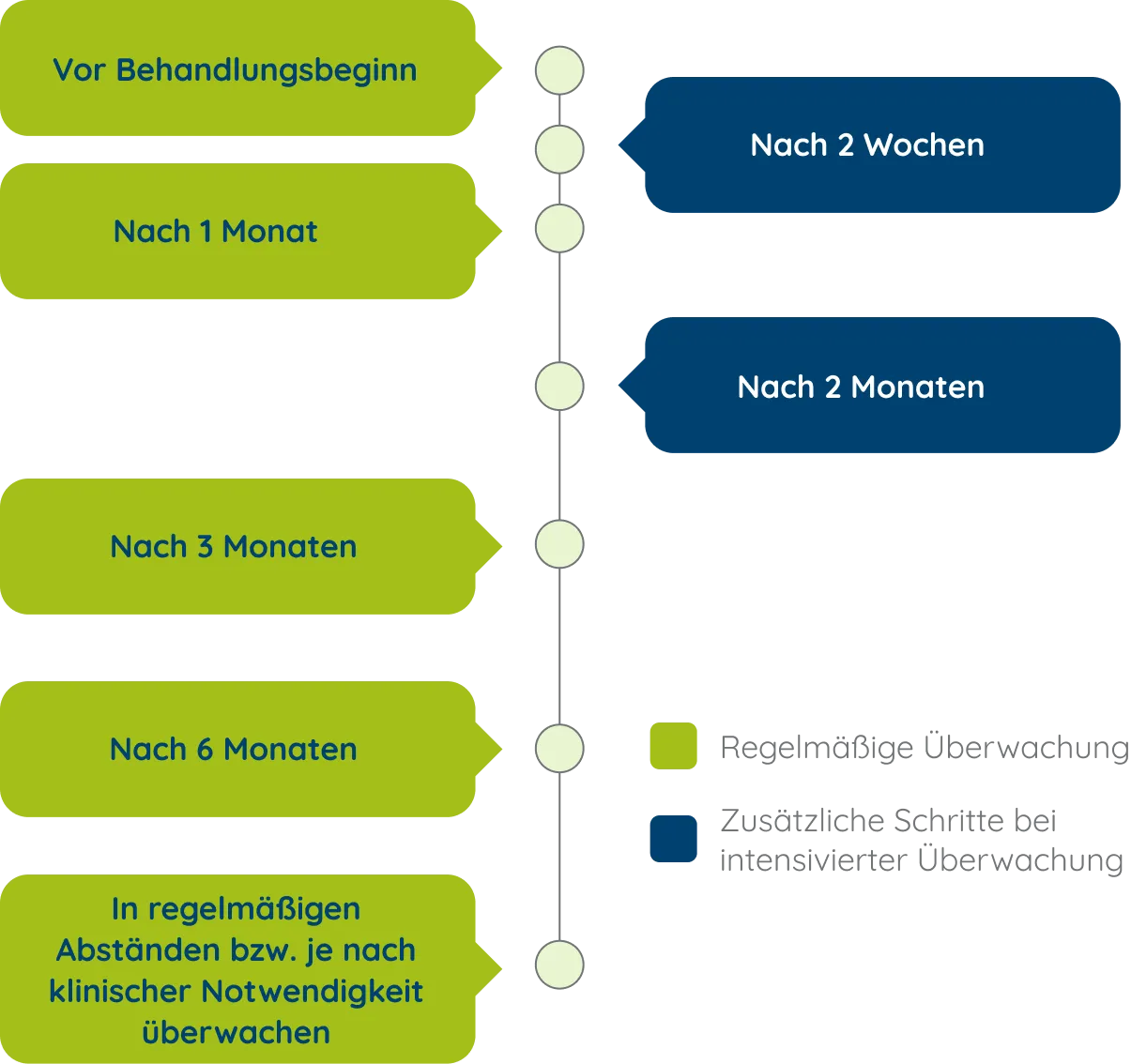
Monitoring-Plan für Patienten, die EPIDYOLEX® erhalten.1
Bei besonderen Patientengruppen sollte die Dosierung von EPIDYOLEX® angepasst werden.1
GUTES VERTRÄGLICHKEITSPROFIL – NACHGEWIESEN ÜBER 3 JAHRE1–5
Nebenwirkungen treten meist am Anfang der Behandlung auf und sind gut beherrschbar:11-14
Die häufigsten mit EPIDYOLEX® assoziierten Nebenwirkungen (≥ 10% aller Patienten) sind:1
- Appetitlosigkeit
- Schläfrigkeit
- Erbrechen
- Fieber
- Durchfall
- Müdigkeit
Die Langzeitverträglichkeit von EPIDYOLEX® zeigte sich in einer Open-Label-Verlängerungsstudie (über 3 Jahre) vergleichbar mit den Ergebnissen aus klinischen Studien zu LGS, DS & TSC.1-5
Abkürzungen
ALT: Alanin-Aminotransferase; ASM: Anfallssuppressives Medikament; AST: Aspartat-Aminotransferase; CBD: Cannabidiol; DS: Dravet-Syndrom; LGS: Lennox-Gastaut-Syndrom; OLE: Open-Label-Verlängerungsstudie; TSC: Tuberöse Sklerose; ULN: oberer Normalwert
* Bei Patienten mit schweren Leberfunktionsstörungen, bei denen der potenzielle Nutzen die Risiken überwiegt, können höhere Dosen von EPIDYOLEX® in Betracht gezogen werden.
- EPIDYOLEX® Fachinformation, aktueller Stand.
- Patel AD, et al. Long-term safety and efficacy of add-on cannabidiol in patients with Lennox-Gastaut syndrome: Results of a long-term open-label extension trial. Epilepsia. 2021;62(9):2228–2239.
- Scheffer IE, et al. Add-on cannabidiol in patients with Dravet syndrome: Results of a long-term open-label extension trial. Epilepsia. 2021;62(10):2505–2517.
- Thiele EA, et al. Long-term cannabidiol treatment for seizures in patients with tuberous sclerosis complex: An open-label extension trial. Epilepsia. 2022;63(2):426–439.
- Thiele EA, et al. Long-Term Safety and Efficacy of Add-on Cannabidiol (CBD) for Seizures Associated with Tuberous Sclerosis Complex (TSC): 3-Year Results from GWPCARE6 Open-Label Extension (OLE) (P14-1.004). Neurology. 2023;100(17_supplement_2):2500.
- Saurer TB, et al. Seizure Outcomes With Cannabidiol (CBD) in Pediatric Versus Adult Patients With Lennox-Gastaut Syndrome (LGS) and Dravet Syndrome (DS): Subgroup Analysis of BECOME, a Caregiver Survey. Neurology. 2023;100(17_supplement_2):P14-1.006.
- Dixon-Salazar T, et al. Nonseizure Outcomes With Cannabidiol in Pediatric Versus Adult Patients With Lennox-Gastaut Syndrome and Dravet Syndrome: Subgroup Analysis of BECOME, a Caregiver Survey. American Epilepsy Society Annual Meeting, 2–6 December 2022. Nashville, TN, USA. Poster 3.429. https://www.gwqrcodes.com/uploads/236750.pdf.
- Seiden LG, Connor GS. The importance of drug titration in the management of patients with epilepsy. Epilepsy Behav. 2022;128:108517.
- Strzelczyk A, Schubert-Bast S. A Practical Guide to the Treatment of Dravet Syndrome with Anti-Seizure Medication. CNS Drugs. 2022;36(3):217–237.
- D’Onofrio G, et al. Slow Titration of Cannabidiol Add-On in Drug-Resistant Epilepsies Can Improve Safety With Maintained Efficacy in an Open-Label Study. Front Neurol. 2020;11:829.
- Privitera M, et al. Time to onset of cannabidiol (CBD) treatment effect in Lennox-Gastaut syndrome: Analysis from two randomized controlled trials. Epilepsia. 2021;62(5):1130–1140.
- Madan Cohen J, et al. Time to onset of cannabidiol treatment effects in Dravet syndrome: Analysis from two randomized controlled trials. Epilepsia. 2021;62(9):2218–2227.
- Wu JY, et al. Time to onset of cannabidiol treatment effect and resolution of adverse events in tuberous sclerosis complex: Post hoc analysis of randomized controlled phase 3 trial GWPCARE6. Epilepsia. 2022;63(5):1189–1199.
- Gunning B, et al. Cannabidiol in conjunction with clobazam: analysis of four randomized controlled trials. Acta Neurol Scand. 2021;143(2):154–163.
Referenzen
- EPIDYOLEX® Fachinformation, aktueller Stand.
- Patel AD, et al. Long-term safety and efficacy of add-on cannabidiol in patients with Lennox-Gastaut syndrome: Results of a long-term open-label extension trial. Epilepsia. 2021;62(9):2228–2239.
- Scheffer IE, et al. Add-on cannabidiol in patients with Dravet syndrome: Results of a long-term open-label extension trial. Epilepsia. 2021;62(10):2505–2517.
- Thiele EA, et al. Long-term cannabidiol treatment for seizures in patients with tuberous sclerosis complex: An open-label extension trial. Epilepsia. 2022;63(2):426–439.
- Thiele EA, et al. Long-Term Safety and Efficacy of Add-on Cannabidiol (CBD) for Seizures Associated with Tuberous Sclerosis Complex (TSC): 3-Year Results from GWPCARE6 Open-Label Extension (OLE) (P14-1.004). Neurology. 2023;100(17_supplement_2):2500.
- Saurer TB, et al. Seizure Outcomes With Cannabidiol (CBD) in Pediatric Versus Adult Patients With Lennox-Gastaut Syndrome (LGS) and Dravet Syndrome (DS): Subgroup Analysis of BECOME, a Caregiver Survey. Neurology. 2023;100(17_supplement_2):P14-1.006.
- Dixon-Salazar T, et al. Nonseizure Outcomes With Cannabidiol in Pediatric Versus Adult Patients With Lennox-Gastaut Syndrome and Dravet Syndrome: Subgroup Analysis of BECOME, a Caregiver Survey. American Epilepsy Society Annual Meeting, 2–6 December 2022. Nashville, TN, USA. Poster 3.429. https://www.gwqrcodes.com/uploads/236750.pdf.
- Seiden LG, Connor GS. The importance of drug titration in the management of patients with epilepsy. Epilepsy Behav. 2022;128:108517.
- Strzelczyk A, Schubert-Bast S. A Practical Guide to the Treatment of Dravet Syndrome with Anti-Seizure Medication. CNS Drugs. 2022;36(3):217–237.
- D’Onofrio G, et al. Slow Titration of Cannabidiol Add-On in Drug-Resistant Epilepsies Can Improve Safety With Maintained Efficacy in an Open-Label Study. Front Neurol. 2020;11:829.
- Privitera M, et al. Time to onset of cannabidiol (CBD) treatment effect in Lennox-Gastaut syndrome: Analysis from two randomized controlled trials. Epilepsia. 2021;62(5):1130–1140.
- Madan Cohen J, et al. Time to onset of cannabidiol treatment effects in Dravet syndrome: Analysis from two randomized controlled trials. Epilepsia. 2021;62(9):2218–2227.
- Wu JY, et al. Time to onset of cannabidiol treatment effect and resolution of adverse events in tuberous sclerosis complex: Post hoc analysis of randomized controlled phase 3 trial GWPCARE6. Epilepsia. 2022;63(5):1189–1199.
- Gunning B, et al. Cannabidiol in conjunction with clobazam: analysis of four randomized controlled trials. Acta Neurol Scand. 2021;143(2):154–163.
Abkürzungen
ALT: Alanin-Aminotransferase; ASM: Anfallssuppressives Medikament; AST: Aspartat-Aminotransferase; CBD: Cannabidiol; DS: Dravet-Syndrom; LGS: Lennox-Gastaut-Syndrom; OLE: Open-Label-Verlängerungsstudie; TSC: Tuberöse Sklerose; ULN: oberer Normalwert
Fußnoten
* Bei Patienten mit schweren Leberfunktionsstörungen, bei denen der potenzielle Nutzen die Risiken überwiegt, können höhere Dosen von EPIDYOLEX® in Betracht gezogen werden.